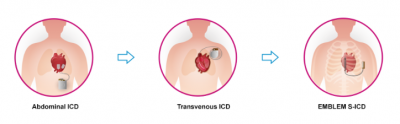
Boston Scientific: I defibrillatori sottocutanei S-ICD Emblemtm da oggi in Italia
i DEFIBRILLATORI SOTTOCUTANEI S-ICD EMBLEMTM compatibili con la RISONANZA MAGNETICA da oggi disponibili anche in Italia
L’introduzione dei nuovi dispositivi, iniziata dopo l’ottenimento del marchio CE, si è completata nel corso dell’estate
 Boston Scientific (NYSE: BSX) ha ricevuto l’approvazione del marchio CE per il nuovo sistema di defibrillatori impiantabili sottocutanei (S-ICD) EMBLEM™ compatibili con la Risonanza Magnetica, nonché l’indicazione di compatibilità con la Risonanza Magnetica per tutti i sistemi S-ICD EMBLEM precedentemente impiantati.
Boston Scientific (NYSE: BSX) ha ricevuto l’approvazione del marchio CE per il nuovo sistema di defibrillatori impiantabili sottocutanei (S-ICD) EMBLEM™ compatibili con la Risonanza Magnetica, nonché l’indicazione di compatibilità con la Risonanza Magnetica per tutti i sistemi S-ICD EMBLEM precedentemente impiantati.
I defibrillatori S-ICD EMBLEM sono opzioni terapeutiche per i pazienti a rischio di arresto cardiaco improvviso (SCA) che lasciano intatti il cuore e i vasi sanguigni e riducono quindi il rischio delle complicanze associate ai tradizionali defibrillatori cardiaci impiantabili transvenosi (TV-ICD). L’introduzione nei mercati, conclusa al termine dell’estate, è avvenuta in due fasi; a quella iniziale, limitata a un gruppo selezionato di Centri Ospedalieri Europei, è seguita la piena distribuzione dei nuovi EMBLEM MRI.
In Europa, il sistema S-ICD EMBLEM MRI amplia la famiglia di dispositivi “ImageReady™” compatibili con la Risonanza Magnetica, con un livello di sicurezza ampio e certificato, purché vengano rispettate le condizioni di impiego nel corso della procedura stessa. I pazienti cui viene impiantato il nuovo sistema S-ICD EMBLEM MRI, così come quelli che abbiano ricevuto in precedenza un sistema S-ICD Emblem, possono ora sottoporsi in piena sicurezza a Risonanza Magnetica “full-body”, termine tecnico che sta ad indicare la possibilità di effettuare l’indagine diagnostica su tutto il corpo del paziente, in ambienti da 1,5 Tesla, laddove le condizioni di utilizzo siano pienamente soddisfatte.
“Queste approvazioni assicurano ai medici e ai loro pazienti l’accesso a esami di RM che si rendessero necessari ed evidenziano l’impegno di Boston Scientific a ottenere l’indicazione di compatibilità con la RM per i dispositivi ad alto voltaggio impiantati oggi”, ha affermato il Dottor Kenneth Stein, Chief Medical Officer, Rhythm Management, Boston Scientific. “Inoltre, il sistema S-ICD EMBLEM è una efficace soluzione terapeutica per la maggior parte dei pazienti per i quali sia indicato l’uso di un defibrillatore impiantabile (ICD), poiché fornisce protezione dall’arresto cardiaco improvviso preservando il cuore e i vasi sanguigni.”
Il sistema S-ICD Emblem MRI presenta due nuove funzioni: la tecnologia “SmartPass” e “Atrial Fibrillation Monitor™”. La tecnologia SmartPass garantisce che il dispositivo entri in funzione solo quando necessario, grazie al potenziamento dell’algoritmo “Insight™” che classifica la frequenza cardiaca per un efficace trattamento dell’aritmia; il nuovo defibrillatore, infatti, individua con precisione sia le aritmie “a rischio” che devono essere affrontate rapidamente, sia quelle fisiologiche, come una tachicardia generata da un’intensa attività fisica, che non necessitano di trattamento. L’algoritmo “Insight™” sarà inoltre disponibile anche nei sistemi S-ICD EMBLEM precedentemente impiantati grazie all’aggiornamento del software, semplice procedura che potrà essere effettuata durante una sessione di follow-up ambulatoriale.
Grazie al sofisticato algoritmo “Atrial Fibrillation Monitor™”, il sistema è anche in grado di individuare precocemente la presenza di Fibrillazione Atriale (FA) e di segnalarla tempestivamente al Centro Ospedaliero di riferimento, permettendo così di ridurre il rischio di insorgenza delle patologie correlate con tale aritmia cardiaca, prima fra queste l’ictus. La FA è un’aritmia che interessa la parte superiore del cuore, cioè le camere atriali, rendendo scoordinata e caotica
l’attività contrattile degli atri, con perdita del movimento e conseguente ristagno di sangue con possibile formazione di coaguli. Quando i coaguli di sangue si spostano possono avanzare fino al cervello, dove rischiano di rimanere intrappolati in un’arteria cerebrale ristretta, bloccando così la circolazione e provocando un ictus. E’ noto che più del 90% dei coaguli di sangue responsabili dell’ictus nei pazienti affetti da FA viene generato in una sacca nella parte sinistra del cuore, chiamata auricola atriale sinistra (LAA).1
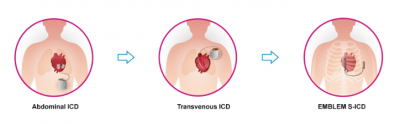 Grazie alle funzioni evolute presenti nella nuova famiglia di defibrillatori sottocutanei EMBLEMTM MRI e alla compatibilita’ con la Risonanza Magnetica, sempre più pazienti potranno beneficiare dell’S-ICD per la prevenzione della morte cardiaca improvvisa, anche quelli ad alto rischio di sviluppare aritmie atriali, prima di tutto la Fibrillazione Atriale, o che per varie ragioni cliniche abbiano maggior necessità di ricorrere ad indagini diagnostiche con Risonanza Magnetica.
Grazie alle funzioni evolute presenti nella nuova famiglia di defibrillatori sottocutanei EMBLEMTM MRI e alla compatibilita’ con la Risonanza Magnetica, sempre più pazienti potranno beneficiare dell’S-ICD per la prevenzione della morte cardiaca improvvisa, anche quelli ad alto rischio di sviluppare aritmie atriali, prima di tutto la Fibrillazione Atriale, o che per varie ragioni cliniche abbiano maggior necessità di ricorrere ad indagini diagnostiche con Risonanza Magnetica.
Per ulteriori informazioni sui sistemi S-ICD EMBLEM: www.sicdsystem.com
Negli Stati Uniti, il sistema S-ICD EMBLEM MRI non è attualmente disponibile in commercio.
Boston Scientific trasforma vite mediante soluzioni mediche innovative che migliorano la salute dei pazienti in tutto il mondo. In qualità di azienda leader a livello mondiale nel settore della tecnologia medica da più di 35 anni, facciamo progredire la scienza per la vita offrendo un’ampia gamma di soluzioni ad alte prestazioni che soddisfano le esigenze irrisolte dei pazienti e riducono la spesa sanitaria.
1 Randall J. Lee, MD, PhD; Krzysztof Bartus, MD; Steven J. Yakubov, MD, Catheter-Based Left Atrial Appendage (LAA) Ligation for the Prevention of Embolic Events Arising From the LAA: Initial Experience in a Canine Model, Circ Cardiovasc Interv 2010;3;224-229.
AVVERTENZA: la legge limita la vendita di questi dispositivi su richiesta o ordine da parte di un medico. Le indicazioni, controindicazioni, avvertenze e istruzioni per l’uso si trovano nel manuale del prodotto fornito con ciascun dispositivo. Le informazioni per l’uso valgono solo nei Paesi con le pertinenti registrazioni del prodotto da parte delle autorità sanitarie e in conformità con le normative locali.
Milano, 31 agosto 2016

